腸内細菌が粘膜の内側まで入るタイミング

腸内細菌は外粘液層にしかいないという常識
腸の中は、菌や食べ物、水分などの通り道としてホース状の空洞になっています。
ホースの内側がいきなり大腸の細胞になっているわけではなく、粘液と粘膜層が外と内を隔てています。
粘液層の中にも、菌たちが比較的自由に出入りできる外粘液層と、より粘度の高い内粘液層があります。
基本的に「健全な腸内では、菌は外粘液層までしか入り込めない」という常識があります。
何かの原因で粘液層が薄くなったり破壊されると、菌たちが大腸の細胞付近にまで押し寄せてしまいます。
その結果、腸の細胞が炎症を起こしたり、最悪の場合は血液に菌が入り込む菌血症を引き起こしたりしてしまいます。
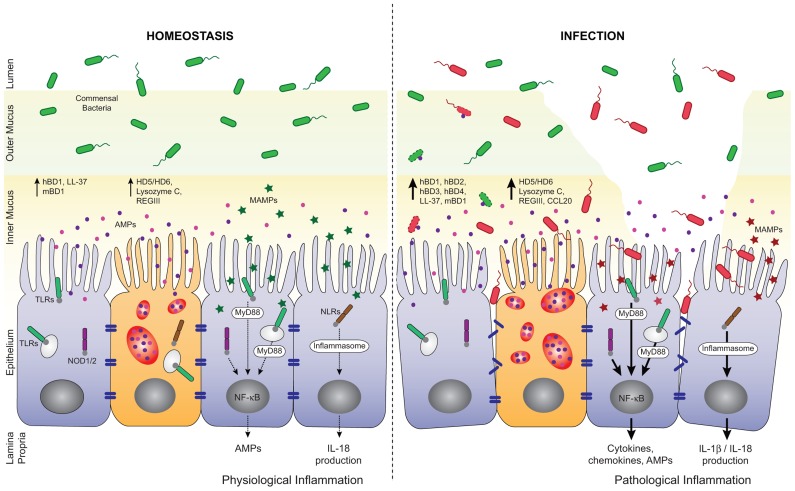
他にも、大阪大学の研究チームが面白い研究結果を発表しています。((Okumura, R., et al. “Lypd8 promotes the segregation of flagellated microbiota and colonic epithelia.” Nature, vol. 532, no. 7597, 2016, pp. 117-121, doi:10.1038/nature17406. Lypd8は鞭毛をもつ細菌と大腸上皮とを分け隔てる : ライフサイエンス 新着論文レビュー))
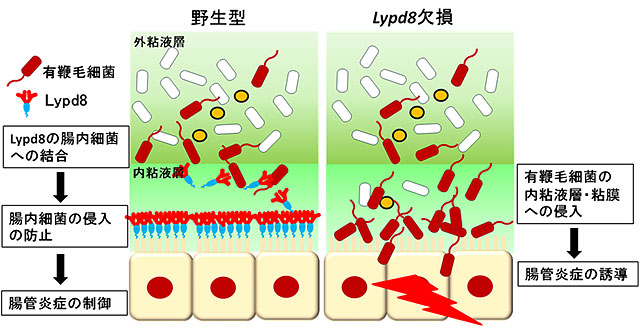
Lypd8という遺伝子が欠損しているマウスでは、内粘液層まで菌たちが侵入してしまうという結果が出ました。
菌が内粘液層、粘膜を通り抜けて大腸の細胞に入り込むのは、決して健全な状態ではありません。
この認識によって、少し誤解もあります。
菌が内粘液層、粘膜下へ入るタイミング
実は、健全な状態だからこそ、菌たちが内粘液層や粘膜下に入るタイミングにもなります。
M細胞を経由した能動的輸送
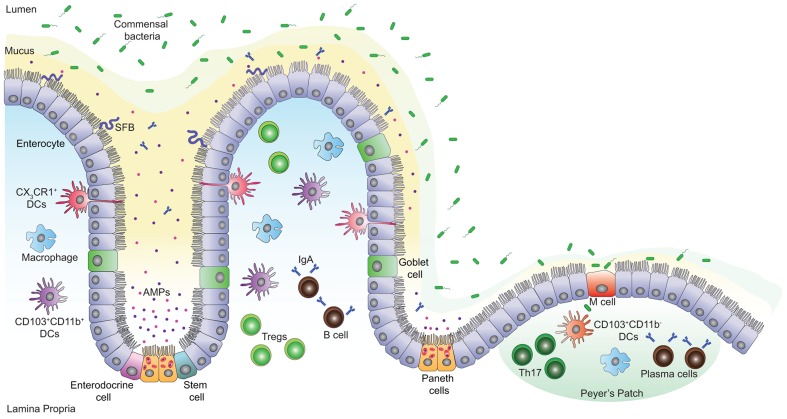
腸の中は、まっすぐな壁ではなく、「絨毛」が多く生えています。
これは腸の表面積を増やすために生えています。絨毛を構成する大腸の細胞たちには、たくさんの種類があります。
赤く光ってるM細胞に注目してみましょう。
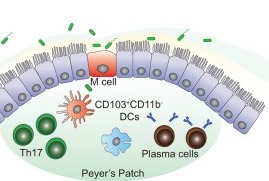
M細胞は、菌が大腸組織内に入るための門のような存在です。
でも門番のように、悪者を追い返したりする役割はあまりありません。
菌(抗原)を樹状細胞という免疫細胞に引き渡します。
このスイッチのメカニズムは明らかにはなっていませんが、TLR(トルライクレセプター)や、菌たちの出す短鎖脂肪酸や、菌とヒトの酵素のやり取りがキーになっているのではないかと思われます。
ちなみに、短鎖脂肪酸のうちの酪酸は、粘液の生成を促す役目もあります。
大腸細胞と距離を保てるように、自分たちで環境を作ります。
T細胞のサイトカイン、B細胞のIgAによる受動的輸送
M細胞から情報を聞いた樹状細胞は、その菌が敵かどうかを判断して、T細胞やB細胞を活性化します。((特殊な腸管上皮細胞、M細胞の生物学))
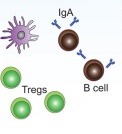
「病原菌がいる!」となれば、Th17細胞による炎症性サイトカインの発令や、キラーT細胞の出動により、菌を排除する方向へ働きます。
逆に「この菌にはぜひ腸に残っていただきたい!」と判断されれば、TregやIgA抗体が出されて、菌たちが腸に留まれるように計らいます。
腸陰窩と杯細胞による菌の輸送?
菌にも大腸組織内に入りやすい入り口とそうじゃない入り口があります。
大阪大学の研究チームの別の論文の画像です。[3]((領域融合レビュー, 5, e007 (2016) DOI: 10.7875/leading.author.5.e007
Ryu Okumura & Kiyoshi Takeda: Crosstalk between intestinal epithelial cells and commensal bacteria.))
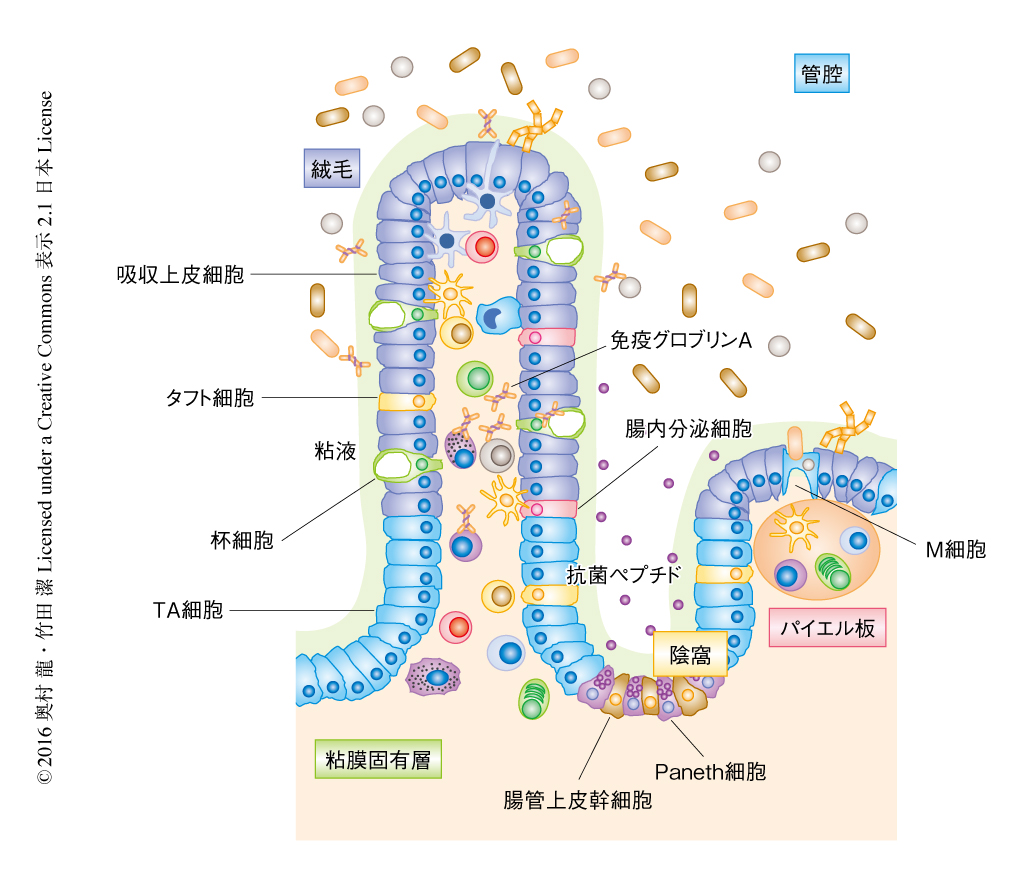
Ryu Okumura & Kiyoshi Takeda: Crosstalk between intestinal epithelial cells and commensal bacteria.より引用
この凹んでるとこ路が陰窩です。
本当は、詰まっていて、粘液も分厚いです。さらに、菌が嫌がるPaneth(パネート)細胞が抗菌ペプチドを出してるため、菌にとって入りにくい環境です。
そのため、この「陰窩」には菌はいないと長年考えられてきました。
でも、この陰窩に特定の菌が大量に住み着いていることがわかってきました。[4]((Pédron, Thierry, et al. “A Crypt-Specific Core Microbiota Resides in the Mouse Colon.” mBio, vol. 3, no. 3, 2012.))
陰窩は入りづらいが、入ってしまうと粘液によって守られている。また、胚細胞という細胞が食事(ムコ多糖類を豊富に含んだ粘液)を提供してくれル。菌にとっては住みやすい環境に変わります。
このエリアからも菌を取り込む可能性があります。
NanoGAS®︎による菌の輸送
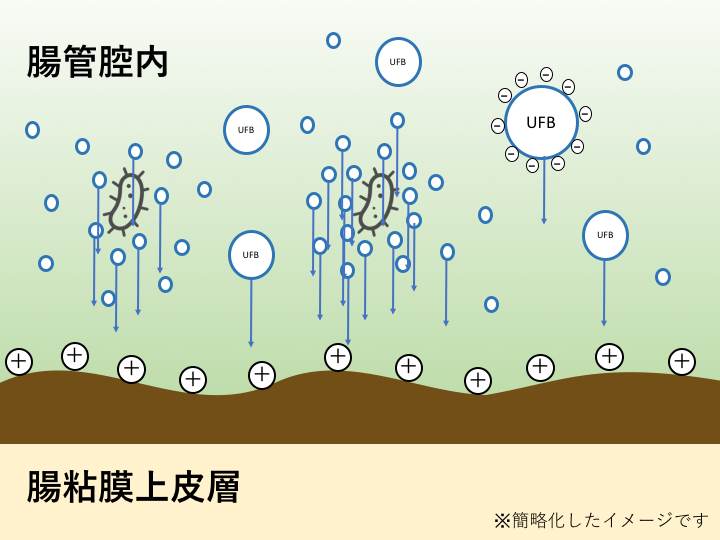
最後に、シンバイオシス株式会社オリジナルの内容です。(参考:《特許出願中》NanoGAS®︎水を使用した移植菌液)
腸内フローラ移植の効果的な方法はいろいろ試されていますが、うちの移植菌液はNNanoGAS®︎というナノバブルを溶媒としています。
通常の生理食塩水を溶媒とするのに比べて、他人由来の腸内細菌の定着を助ける目的です。
菌が腸に残っていいかどうかを判断するために叩く扉、M細胞は狭き門です。まずは移植した菌たちがこの扉までスムーズにたどり着けるよう、ナノバブルが手伝います。
菌たち同士の生物活性電位、NanoGAS®︎の持つウルトラファインバブル(UFB)特有の電位などが関わります。しかし、そのメカニズムは検証段階です。
生化学と、生物学と、物理工学と、理論物理が混ざったようなメカニズムです。
その他の ブログ に関する記事
Articles about other ブログ

2021年10月26日
FMTのゴールは? 移植回数と事前抗生剤投与が菌の生着に与える影響
移植回数と事前抗生剤投与が菌の生着に与える影響 原文Microorganisms | Free Full-Text | Engraftment of Bacteria after Fecal Microbiota Tra […]

2021年08月03日
腸内細菌が粘膜の内側まで入るタイミング
腸内細菌は外粘液層にしかいないという常識 腸の中は、菌や食べ物、水分などの通り道としてホース状の空洞になっています。ホースの内側がいきなり大腸の細胞になっているわけではなく、粘液と粘膜層が外と内を隔てています。 粘液層の […]
2021年05月31日
パーキンソン病や耐性菌にFMTが有効
FMTがパーキンソン病の症状を緩和 (原文)Evaluation of fecal microbiota transplantation in Parkinson’s disease patients wit […]




